随着新型冠状病毒疫苗的推出,人工智能(Artificial Intelligence,AI)在药物研发中越发不可或缺。目前,国内外学者、研究院已经广泛开展人工智能技术用于新冠疫苗研发的研究,因为AI平台可以通过大数据处理、机器学习等技术对有效控制SARS-CoV,SARS-CoV-2和HIV病毒的化合物进行分析利用,从而鉴定具有抑制人类冠状病毒活性的药物。人工智能作为新一代信息技术,也将成为在我国“十四五”期间为推动经济发展,助力疾病医治预测,创新药物、医疗器械研发应用的核心驱动力之一。
1. 人工智能的概念
人工智能这个概念已经不再陌生,通常是指通过计算机程序或者系统来呈现人类思维和智能的技术。人工智能通过抓取数据中存在的概念和关系,独立分析学习数据模式从而达到模拟人类思维的目的。人工智能主要涉及的方法领域包括推理、知识表达、搜索解决方案以及机器学习(Machine Learning)。
德勤咨询报告将机器学习划分为广义的人工智能技术,并定义为“从结构化和非结构化数据中学习、识别隐藏模式、进行分类并预测未来结果的计算机算法。”机器学习技术包括深度学习(Deep Learning),是一种基于机器学习的方法,利用一种类似于大脑的逻辑结构(称为神经“网络”),来识别和区分语音、图像和视频等模式。自然语言处理(Natural language processing,NLP)是深度学习的一种,是计算机技术在自然语言和语音分析与合成中的应用。
2. AI在新药研发中的具体应用
新药研发是个漫长而复杂的过程,伴随着高昂的研发成本、精力以及高度不确定性。有学者统计,一个新药从研发初期到上市,可能需要数十年,消耗资金可多达30亿美元。典型的新药研发过程通常包括:1)早期的目标识别及靶点、最优化合物确认;2)临床前研究;3)临床研究I、II、III期阶段;以及4)食药监局审批。在化学世界里,潜在药物分子多达1060个,因此发现新药可以说如同大海捞针。近年来,传统的新药研发越来越难,研发投资和研发时间也不断增加。新药研发处于一个难以突破的瓶颈阶段,急需借助于新的技术来帮助新药研发的不断突破。
人工智能凭借其强大的自适应特征和学习能力,通过算法、推演等技术核心可以应用到新药研发的各个环节,在保证分析质量的同时,可实现大幅降低药物研发成本, 缩短研发时间,提高研发效率,使新药开发走上快速高效的道路。
Tekade博士及其团队于2020在《Drug Discovery Today》期刊上发表的一篇文献里总结到人工智能技术在新药研发的五个重要部分都有不可估量的潜力:

下面从这几个AI在医药行业实际应用的领域作详细的介绍:
(1) 药物设计
预测靶点蛋白3D结构
蛋白质功能紊乱是导致许多疾病的重要因素,因此在新药研发第一步靶点识别和确认中,找到药物在体内的作用靶点,确定靶点蛋白质结构从而针对性设计药物分子来调节蛋白功能是至关重要的基石。蛋白质的三维结构由一系列氨基酸折叠而成,由于根据最稳态原理推测出蛋白质三维结构需要考虑到其各个原子间的相互作用力,因此巨大的计算量使得测定蛋白质结构往往需要很长的周期、经费且难度大。
到目前为止,在“生命体中已知的约2亿种氨基酸序列中,只有约17万种蛋白质结构得以确定”。尽管如此,对于已经存在大量数据的氨基酸序列,人工智能已经被研究学者用于预测蛋白质结构。Spencer等人在2015年通过采用deep learning network architectures(DNSS)对198个蛋白质进行完全独立测试,预测第二级蛋白质结构准确率达到了80.7%。Wang博士及其团队在2016年发表于《自然》的文献里介绍到一种叫DeepCNF(Deep Convolutional Neutral Fields)的人工智能技术用于预测蛋白质的第二级结构。DeepCNF技术不仅可以通过深度层次结构对复杂的序列与结构关系建模,还可以对相邻的蛋白质第二级结构标签之间的相互依赖性进行建模。实验结果证明该技术可实现84%的预测准确率,并可以扩展到对蛋白质的其他结构性质,比如接触数、无序区域以及溶剂可及性。去年11月30日,谷歌旗下的DeepMind公司AlphaFold人工智能系统在国际蛋白质结构预测竞赛(Critical Assessment of Structure Prediction,CASP)上以绝对的优势夺冠,其预测的蛋白质三维结构与实验方法解析的结构几乎完全吻合,在最具挑战的蛋白质结构预测上也获得将近90分的成绩,而其他参赛队伍最好的成绩也只有75分。由此可见,人工智能技术在实现蛋白质结构的精准预测有巨大潜力,将会为新药研发带来前所未有的技术革新从而提高研发效率。
预测药物和蛋白质相互作用
决定药物的靶蛋白,也被称作药物和蛋白质的相互作用(drug-protein interaction,DPI),在药物研发过程中有着极其重要的作用:通过预测药物与受体或者蛋白质的相互作用,可以帮助理解药物的功效、效力,从而对药物进行最有效的设计。
得益于越发丰富的数据库(例如化合物集中的数据库PubChem、ChEMBL以及DUD-E,蛋白质集中的数据库UniProt和PDBbind以及整合数据库BindingDB)许多研究学者已经采用不同的人工智能技术对配基-蛋白质的相互作用成功进行预测。Wang博士等人采用Support Vector Machine(SVM,一种按监督学习的方式对数据进行二向分类的广义线性分类器),对存在于626个蛋白质和10000个活跃化合物里15000个配基-蛋白质的相互作用进行训练,成功地发现了4种重要药理靶点(GPR4,SIRT1,p38,and GSK-3β)的9种新型活性化合物。
(2) 化学合成
新药研发高成本很大一部分可能归因于两个因素:经过临床试验的候选分子的高损耗率(损耗率超过85%)和前一个研发阶段的复杂性,这需要大量的时间和资源投资。如果一家制药公司拥有更强大的临床前候选药物管道,这将在药物总批准方面产生有益的下游效应。因此,采用先进的计算机硬件和计算机方法加快以及提高药物化学在药物新药发现循环下各个方面的表现-design-make-test-analyze (DMTA)。这其中,研究学者越来越感兴趣的一个领域是使用数据驱动合成预测工具使阶段加速和减少新分子实体合成的失败。
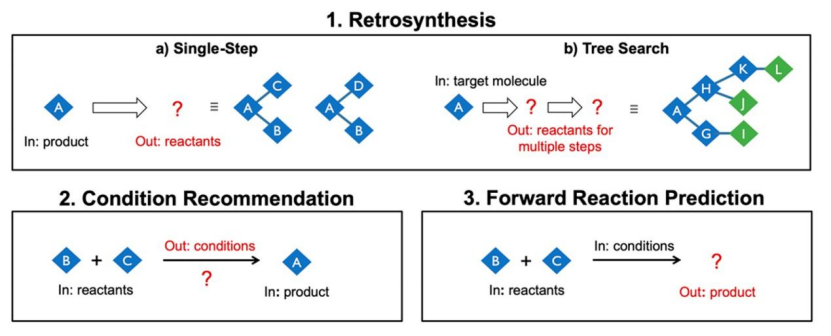
计算机辅助化学合成综合规划的三个主要任务包括:
(1)逆合成可以分解为以下问题:
(a)每次一步生成反合成建议和
(b)递归使用单步建议来识别完整的多步路线。
(2)为了使建议可行,必须提出能导致成功正向反应的反应条件。
(3)反应预测,从一组起始原料和条件预测可能的产物,用于验证所提出的合成步骤。
(3) 药物再利用
药物再利用或者药物再定位(drug repurposing)指将已上市的药物,包括正在进行研究的药物和临床失败的药物,用于原定用途之外的疾病治疗的过程。正如诺贝尔奖获得者药理学家Sir James Black的一句名言所说: “发现新药最富有成效的基础就是老药(The most fruitful basis of the discovery of a new drug is to start with an old drug)”。得益于老药已知的安全性,药物再利用不仅可以大幅度降低研发成本,还可以有效减少药物安全性测试的相关的风险,因此也是新药研发中比较重要的一种研发策略。
如今,人工智能技术已经被广泛用于药物再利用的系统研发过程中。Steve Rodriguez 和他的团队开发的机器学习框架-DRIAD (Drug Repurposing in AD)能够量化阿尔兹海默症的严重程度(Braak阶段)的病理和分子机制之间的潜在联系,该研究通过对80种主要含抗癌活性的激酶抑制剂(其中33种已经FDA批准并经临床测试)进行体外分析,将DRIAD用于分析由这80种化合物产生的基因列表,产生一个可能的再利用候选药物的排名列表。 DRIAD需要两类输入信息进行学习 – 阿尔兹海默症不同发展阶段人类大脑的mRNA表达情况以及由神经元细胞差异表达的基因组成的序列。由于在进行模型训练和预测评估之前,DRIAD就已经分离出基因表达富集与预测性能,因此该人工智能框架能够提供更直接、更客观的量化结果。
Zhou Yadi博士等人在《柳叶刀》发表的一篇文献中总结到不同人工智能技术用于药物再利用的研究,尤其将老药用于新冠肺炎(COVID-19)的治疗的可能性。这些技术包括前馈神经网络(Feedforward Neural Network)、主要分析处理图像输入变量的卷积神经网络(Convolutional Neural Network),更适合处理生物序列的循环神经网络(Recurrent neural networks)以及图表表征学习(Graph representation learning)。通过人工智能技术(药物网络分析)发现可能用于新冠肺炎治疗的候选药物包括托瑞米芬(Toremifene),一款于1997年被批准用于治疗乳腺癌的第一代雌激素受体调节剂。体外实验表明,托瑞米芬在微摩尔浓度下可阻断病毒感染,包括中东呼吸综合征冠状病毒、新型冠状病毒SARS-CoV-2。经过Benevolent AI公司的知识网络图谱分析与识别,巴瑞替尼(Baricitinib)也被认为对治疗新冠肺炎的有一定功效。目前,至少2项以巴瑞替尼单独或与抗病毒药物联合治疗的用于中度和重度的新冠肺炎患者的双盲试验临床II期正在美国进行。
(4) 多重药理学
在现代药物研发领域,大多数治疗方法都是通过调节多个靶标和通路来达到预期效果。根据美国国家医学图书馆的定义,多重药理学是“对作用于多个靶点或疾病途径的药剂的设计或使用”。如癌症、阿尔茨海默症等复杂疾病通常由环境、遗传等多种因素共用作用的复杂机制引起的。因此,多重药理学已经被提出并成为一种强大和有前途的替代范式,用于开发多种治疗药物,以满足迫切的医疗求。
虽然在过去多靶点药物的鉴定主要是偶然的,随着化学生物学和计算机科学的发展,使药物多重药理学的合理设计成为可能。特别是,现代体外高通量/高含量筛选和体内动物模型技术加快了对药物靶点组合的系统识别,而在电脑模拟(in silico)方法中,结构体学和药物化学使多靶点药物的有效设计成为可能。
基于配体的药物多药理学预测方法主要依赖于其化学结构和生物活性。最近,Lee等利用1121个靶点,利用人工智能随机森林方法开发了基于配体的靶点预测模型。结果显示,对于前1%和前3%的目标,他们的回忆率分别达到了67.6%和73.9%。
总部位于加拿大多伦多的生物科技公司Cyclica专门采用多药理学方法进行药物发现,将药物分子的所有潜在靶标相互作用作为首要考虑因素。Cyclica的集成人工智能(AI)增强药物发现平台能够对具有良好多重药理特征和药用特性的候选药物进行多目标评估和设计。不同于传统计算机辅助药物设计的方法(如侧重于基于结构的生物物理学以及基于知识)需要在有大量数据存在的分子类别和蛋白质靶标上发挥最大作用,Cylica的平台促进了针对特征不太明确的蛋白质的分子设计,同时也揭示了分子的作用机制。Cyclica平台将目标反褶积应用于药物再利用和重新设计。该平台由两个机器学习引擎MatchMaker和POEM提供动力。
(5) 药物筛选
虚拟筛选(virtual screening)是计算机辅助药物设计中一种重要的开发工具。利用小分子化合物与药物靶点间的分子对接运算,虚拟筛选可以从庞大的分子中快速遴选出活性化合物。传统的高通量筛选技术(High-throughput screening)存在高成本、低成功率的问题,虚拟筛选则可通过在早期药物研发时过滤掉结构不合适的化合物,提高化合物筛选效率,从而缩短研究周期,降低药物研发的成本。
虚拟筛选主要的两种方法有基于配体的虚拟筛选(ligand-based virtual screening,LBVS)与基于受体的虚拟筛选(structure-based virtual screening,SBVS)。前者不依赖三维蛋白质结构信息,而是基于活性及非活性配体的实证数据,利用活性配体之间的化学和空间相似性及物理化学分析来预测和识别其他具有高生物活性的配体。传统的机器学习方法,例如SVM、KNN、Boosting以及NB,被大量运用在LBVS中。而SBVS则依赖于实验测定的或同源模建的受体生物大分子的三维结构,主要用于研究可能的活性配体与结合为点残基间的相互作用。 SBVS通过打分函数对蛋白和小分子化合物的结合能力进行评价,最终从大量的化合物分子中挑选出结合模式比较合理的、预测得分较高的化合物,往往比LBVS有更好的预测表现。
3. AI在实际药物研发中的成功案例
截止2021年四月十二日,据BiopharmaTrend.com网站统计,专注人工智能技术进行药物开发与研究的公司已达到270家,分散于10个不同领域,包括化学合成、靶点/先导化合物确认、临床前研究、药物再利用等。
人工智能公司与国际大型药企的合作已经屡见不鲜,许多国际大药企就不同药物研发领域同人工智能公司展开相应的战略合作。GlaxoSmithKline (GSK)在2017年同美国的Insilico Medicine达成合作协议,希望借助后者的人工智能平台发现新的药物靶点及通路。2017年6月,Genentech宣布与GNS Healthcare进行研究合作,利用该公司自有的REFS机器学习和模拟AI平台去识别与验证新的癌症药物靶点。武田制药也宣布同人工智能药物设计公司Numerate进行多年研究合作,专注开发肿瘤学、胃肠病学和中枢神经系统疾病的新临床候选药物。本篇文章重点介绍两家人工智能公司Exscientia和BenevolentAI,及其人工智能技术在药物研发中已经取得的一些成果。
Exscientia
Exscientia是一家位于英国牛津,通过端对端的人工智能平台对药物进行设计制药科技公司,也是首家实现药物设计自动化的公司。许多国际大药企已经分别与Exscientia达成战略合作:2017,GSK与Exscientia签署研究协议就GSK筛选的10个疾病靶点通过人工智能平台开发小分子药物,并且针对这些靶点发现临床候选药,如果所有里程碑Exscientia都实现,则会获得GSK提供的3300万英镑的研究资金。同年,赛诺菲出资2.73亿美元,与Exscientia共同开发治疗糖尿病及其并发症的双特异小分子药物,涉及领域包括血糖控制、非酒精性脂肪肝、体重管理及其他代谢方面的疾病。双方已经筛选了45个单靶点和1000个双靶点组合,随后会借助Exscientia的人工智能平台剔除掉在化学上难以处理的组合。拜耳和Exscientia于2020年初签署一份为期三年价值2.4亿欧元的合作协议,通过结合Exscientia的人工智能药物研发平台以及拜耳的数据,专注药物早期研究、识别及优化治疗心血管疾病和肿瘤疾病的先导化合物。
许多与Exscientia合作的制药公司在新药研发方面已经取得了一些进展。2020年1月30日,日本住友制药协会与Exscientia合作开发的首个AI设计的新药,用于治疗强迫症的DSP-1181已经在日本开展I期临床试验。该药物的设计借助于住友制药在G蛋白偶联受体方面的药物研发经验以及Exscientia的Centaur Chemist™人工智能平台,将探索性研究所需时间大幅缩短至12个月以内,而用传统办法进行的研究平均则需4.5年。2021年4月9日,Exscientia宣布与Evotec共同合作研发的由AI设计的肿瘤免疫分子即将进入临床试验。该肿瘤免疫分子是一款A2A受体拮抗剂(EXS21546),用于治疗成人晚期实体瘤,通过研究EXS21546证明了A2A受体的活性足以在高浓度腺苷类似物存在的情况下完全恢复T细胞功能。此外,Exscientia的CEO Andrew Hopkins博士还表示“尽管我们为这个项目设立了具有挑战性的目标-对A2A受体的高选择性和中枢神经系统保留特性从而减少全身副作用,还是可以在项目启动后的8个月内发现候选药物分子。”
Benevolent AI
Benevolent AI是一家成立于英国伦敦的独角兽公司,其主要利用人工智能技术,从各种结构化以及非结构化的生物医学数据源中提取数据并整理、归纳、标准化,通过将数据输入到公司的专利知识图谱中,从而提取出能够推动药物研发的知识而加速药物研发的过程。
阿斯利康与Benevolent AI于2019年达成战略合作,结合阿斯利康自有的基因组学、化学以及临床数据与Benevolent AI靶点识别平台和生物医学知识图谱,对治疗慢性肾病和特发性肺纤维化疾病方面的药物进行新药研发。该合作在2021年1月27日取得了阶段性的成功,阿斯利康在Benevolent AI的人工智能技术帮助下,在导致慢性肾病的潜在细胞机制中,成功发现了新的额药物靶点,并已将该靶点纳入其公司药物开发计划,准备进一步的药物研发。
目前,Benevolent AI药物研发项目主要涵盖过敏性皮肤炎、肌萎缩性脊髓侧索硬化症、溃疡性结肠炎、炎症性肠病、中枢神经系统疾病、胶质母细胞瘤、非酒精性脂肪肝,同阿斯利康合作的慢性肾病、特发性肺纤维化疾病以及20多个早期药物靶点探究。其中,通过其人工智能平台研发治疗过敏性皮肤炎的药物BEN-2293已经进入I期临床试验,该药物被视作是一款best-in-class、通过AI技术研发的多靶点小分子Pan-Trk拮抗剂。
4. 挑战和思考
AI在药物发现中的挑战
尽管人工智能在药物发现方面显示出了巨大的希望,但并非没有挑战。 AI面临着数据缺失、互操作性缺失等诸多挑战。
在所有实施人工智能的行业中,缺乏数据是一个反复出现的问题。在传统的生物学研究中,有效样本的数量有限。 然而大多数机器学习算法必须在成百上千的数据点或样本上进行训练才能表现良好。另一个挑战是缺乏可解释性。通常很难解释模型如何进行某些预测和执行。更可能发生在深度学习中,其中每一层都增加了模型的复杂性。随着层数的增加,对每一层输出的解释可能会变得指数级复杂。
使用人工智能预测药物靶点的另一个障碍仍然是将全球实验室进行的传统基础研究翻译成计算机可以理解的语言。机器学习程序依赖于以可以识别模式并可以训练机器的格式呈现的数据。这通常需要复杂的实验设计,将人为错误保持在最低限度,并且可以在几乎相同的条件下执行多次不同的实验迭代。
机器学习算法将数据转换为通路检测、3D 蛋白质结构、代谢物质量测量等。这些 AI 转换可以以前所未有的速度发生。然而,在许多情况下,所使用的数据质量不佳(例如图像分辨率)或不平衡(即来自罕见疾病的样本在数据集中代表性不足)。
与任何给我们对现有技术的理解带来范式转变的进步一样,人工智能仍然无法在药物发现过程中完全取代人类科学家。最终,计算机的预测必须经过科学家的验证,以确保人工智能在药物研发在的有效性和实用性。
思考与未来
人工智能技术在新药研发中有巨大的前景,而且有些技术已经取得了阶段性的进展,AI协助研发出来的新药也已经进入临床,不少AI医药研发公司也在不断的取得新的成果。但是,AI技术在医药研发上若要取得井喷性和长期有效的成果,还需要有更大的改善和发展。
人工智能技术在新药研发的应用是一项跨学科,跨行业的合作,极需具备精通人工智能技术及生物制药技术的复合型人才, 也需要IT行业与医药行业,学校及科研机构与医药公司的通力合作。国际制药大公司可以通过其雄厚的研发力量在这方面取得成果。中小型的医药研发公司也可以找准目标,确定突破口,同时积累人才,做好转型转化的工作,取得快速有成效的成果。
人工智能技术在新药研发要取得持久的研发成果和商业价值,也需要医药公司与投资行业的紧密合作。 只有大规模的投资进入这个领域,营造出良好的行业状态和环境,才能使人工智能技术在新药研发从初期的探索,走向中期大规模产品进入临床试验,最终产品进入商业市场,为患者快速带来急需的医药产品,为研发者和投资者带来回报。
参考资料:
1. Ke, Y.-Y., Peng, T.-T., Yeh, T.-K., Huang, W.-Z., Chang, S.-E., Wu, S.-H., Hung, H.-C., Hsu, T.-A., Lee, S.-J., Song, J.-S., 2020. Artificial intelligence approach fighting COVID-19 with repurposing drugs. Biomed. J. https://doi.org/10.1016/ j.bj.2020.05.001.
2. 德勤(2020),“十四五”规划的思考. https://www2.deloitte.com/content/dam/Deloitte/cn/Documents/ser-soe-br/deloitte-cn-fourteenth-five-year-plan-report-zh-200521.pdf
3. 工联网,中国信通院解读:“十四五”规划人工智能三大布局,2021.03.17. http://www.cww.net.cn/article?id=484079
4. 德勤(2020),“十四五”规划的思考. https://www2.deloitte.com/content/dam/Deloitte/cn/Documents/ser-soe-br/deloitte-cn-fourteenth-five-year-plan-report-zh-200521.pdf.
5. Paul, Debleena et al. “Artificial intelligence in drug discovery and development.” Drug discovery today vol. 26,1 (2021): 80-93. doi:10.1016/j.drudis.2020.10.010
6. https://www2.deloitte.com/content/dam/insights/us/articles/32961_intelligent-drug-discovery/DI_Intelligent-Drug-Discovery.pdf
7. Claudio N. Cavasotto, Juan I. Di Filippo, Artificial intelligence in the early stages of drug discovery, Archives of Biochemistry and Biophysics, Volume 698, 2021, 108730, ISSN 0003-9861,
8. https://doi.org/10.1016/j.abb.2020.108730.
9. Debleena Paul, Rakesh K. Tekade, et al. Artificial intelligence in drug discovery and development, Drug Discovery Today, Volume 26, Issue 1, 2021, Pages 80-93, ISSN 1359-6446, https://doi.org/10.1016/j.drudis.2020.10.010.
10. http://stcsm.sh.gov.cn/xwzx/kjzl/20210112/fecb48d476b94fa4aca8798dd83db1b8.html
11. https://finance.sina.com.cn/chanjing/gsnews/2020-12-01/doc-iiznctke4188648.shtml
12. Liangliang Wang, Junjie Ding, Li Pan, Dongsheng Cao, Hui Jiang, Xiaoqin Ding, Artificial intelligence facilitates drug design in the big data era, Chemometrics and Intelligent Laboratory Systems, Volume 194, 2019, 103850, ISSN 0169-7439, https://doi.org/10.1016/j.chemolab.2019.103850.
13. M. Spencer, J. Eickholt, J.L. Cheng, A deep learning network approach to ab initio protein secondary structure prediction, IEEE/ACM Trans. Comput. Biol., 12 (2015), pp. 103-112, https://doi.org/10.1109/tcbb.2014.2343960.
14. Wang, S., Peng, J., Ma, J. et al. Protein Secondary Structure Prediction Using Deep Convolutional Neural Fields. Sci Rep 6, 18962 (2016). https://doi.org/10.1038/srep18962
15. Nature, “It will change everything’: DeepMind’s AI makes gigantic leap in solving protein structures”, 30 November 2020, https://www.nature.com/articles/d41586-020-03348-4
16. Debleena Paul, Rakesh K. Tekade, et al. Artificial intelligence in drug discovery and development, Drug Discovery Today, Volume 26, Issue 1, 2021, Pages 80-93, ISSN 1359-6446, https://doi.org/10.1016/j.drudis.2020.10.010.
17. Sangsoo Lim, Yijingxiu Lu, et al. A review on compound-protein interaction prediction mehods: Data, format, representation and model, Computational and Structural Biotechnology Journal, Volume 19, 2021, Pages 1541-1556, ISSN 2001-0370, https://doi.org/10.1016/j.csbj.2021.03.004.
18. Wang, F. et al. (2011) Computational screening for active compounds targeting protein sequences: methodology and experimental validation. J. Chem. Inf. Model. 51, 2821–2828
19. J. Med. Chem. 2020, 63, 16, 8667–8682 Publication Date: April 3, 2020 https://doi.org/10.1021/acs.jmedchem.9b02120
20. Zhou Y, Wang F, Tang J, Nussinov R, Cheng F. Artificial intelligence in COVID-19 drug repurposing. Lancet Digit Health. 2020 Dec;2(12):e667-e676. doi: 10.1016/S2589-7500(20)30192-8. Epub 2020 Sep 18. PMID: 32984792; PMCID: PMC7500917.
21. Kettle JG, Wilson DM. Standing on the shoulders of giants: a retrospective analysis of kinase drug discovery at AstraZeneca. Drug Discov Today. 2016 Oct;21(10):1596-1608. doi: 10.1016/j.drudis.2016.06.007. Epub 2016 Jun 15. PMID: 27319293.
22. Liangliang Wang, Junjie Ding, Li Pan, Dongsheng Cao, Hui Jiang, Xiaoqin Ding, Artificial intelligence facilitates drug design in the big data era, Chemometrics and Intelligent Laboratory Systems, Volume 194, 2019, 103850, ISSN 0169-7439, https://doi.org/10.1016/j.chemolab.2019.103850.
23. Rodriguez, S., Hug, C., Todorov, P. et al. Machine learning identifies candidates for drug repurposing in Alzheimer’s disease. Nat Commun 12, 1033 (2021). https://doi.org/10.1038/s41467-021-21330-0
24. Zhou Y, Wang F, Tang J, Nussinov R, Cheng F. Artificial intelligence in COVID-19 drug repurposing. Lancet Digit Health. 2020 Dec;2(12):e667-e676. doi: 10.1016/S2589-7500(20)30192-8. Epub 2020 Sep 18. PMID: 32984792; PMCID: PMC7500917.
25. https://www.tandfonline.com/doi/full/10.1080/17460441.2020.1767063
26. Lee K, Lee M, Kim D. Utilizing random Forest QSAR models with optimized parameters for target identification and its application to target-fishing server. BMC Bioinformatics. 2017 Dec 28;18(Suppl 16):567. PubMed PMID: 29297315; PubMed Central PMCID: PMCPMC5751401.
27. https://www.nature.com/articles/d43747-020-01098-w
28. Liangliang Wang, Junjie Ding, Li Pan, Dongsheng Cao, Hui Jiang, Xiaoqin Ding, Artificial intelligence facilitates drug design in the big data era, Chemometrics and Intelligent Laboratory Systems, Volume 194, 2019, 103850, ISSN 0169-7439, https://doi.org/10.1016/j.chemolab.2019.103850.
29. https://www.medchemexpress.cn/virtual-screening.html
30. https://www.biopharmatrend.com/m/companies/ai/
31. https://www.biopharmatrend.com/post/34-biopharmas-hunt-for-artificial-intelligence-who-does-what/
32. https://www.fiercebiotech.com/medtech/gsk-exscientia-ink-ai-based-drug-discovery-deal-worth-up-to-42m
33. https://media.bayer.com/baynews/baynews.nsf/id/Bayer-Exscientia-collaborate-leverage-potential-artificial-intelligence-cardiovascular-oncology
34. https://www.exscientia.ai/news-insights/sumitomo-dainippon-pharma-and-exscientia-joint-development
35. https://www.exscientia.ai/news-insights/aacr-presentation-exs21546-non-cns-penetrant-a2ar-selective-antagonist
36. https://www.exscientia.ai/news-insights/exscientia-first-ai-designed-immuno-oncology-drug-trial
37. https://www.benevolent.com/what-we-do
38. https://www.astrazeneca.com/media-centre/press-releases/2019/astrazeneca-starts-artificial-intelligence-collaboration-to-accelerate-drug-discovery-30042019.html
39. https://www.prnewswire.com/news-releases/benevolentai-and-astrazeneca-achieve-collaboration-milestone-with-novel-ai-generated-chronic-kidney-disease-target-301215406.html
40. https://www.benevolent.com/benevolentai-drug-programmes
42. https://roboticsbiz.com/ai-in-drug-discovery-benefits-drawback-and-challenges/